NEWS
新聞資訊
科研合作
乳腺癌是全球女性中最常見(jiàn)的惡性腫瘤之一,治療方法隨著科技進(jìn)步不斷更新。從手術(shù)到放療、化療,再到靶向、免疫治療和ADC,患者的生存率和生活質(zhì)量有了明顯改善。本文將全面介紹乳腺癌治療歷程,并重點(diǎn)討論三陰性乳腺癌(TNBC)的免疫治療新進(jìn)展。
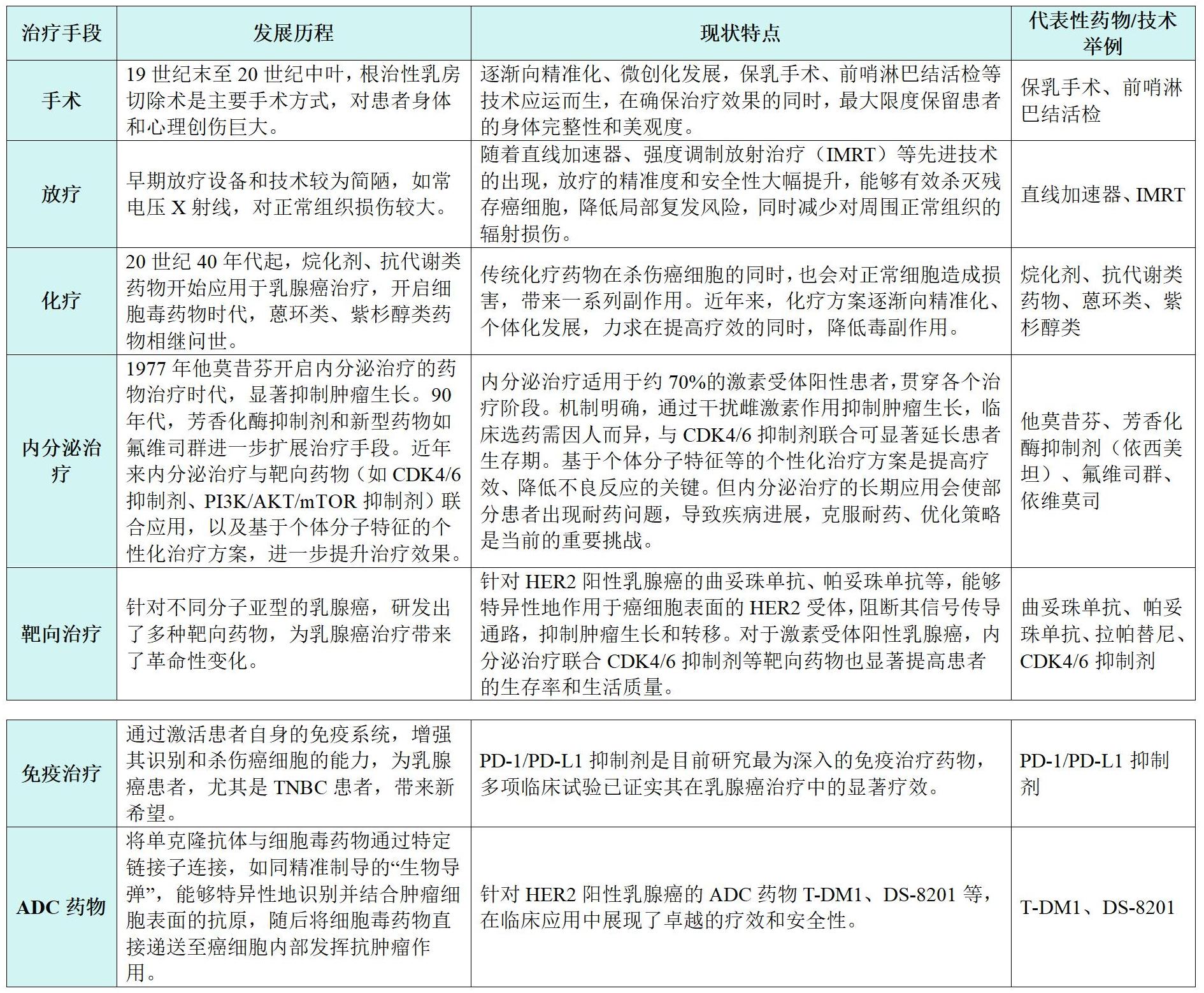
三陰性乳腺癌(TNBC)約占所有乳腺癌病例的15%-20%,因其缺乏雌激素受體(ER)、孕激素受體(PR)和人表皮生長(zhǎng)因子受體2(HER2)的表達(dá),傳統(tǒng)內(nèi)分泌治療和HER2靶向治療對(duì)其無(wú)效,治療手段主要依賴(lài)化療,預(yù)后較差。近年來(lái),免疫治療在TNBC領(lǐng)域取得了顯著突破,成為研究和臨床應(yīng)用的熱點(diǎn)。
多項(xiàng)大型臨床試驗(yàn)探索了免疫治療在TNBC中的應(yīng)用,主要集中在PD-1/PD-L1抑制劑聯(lián)合化療的方案上。
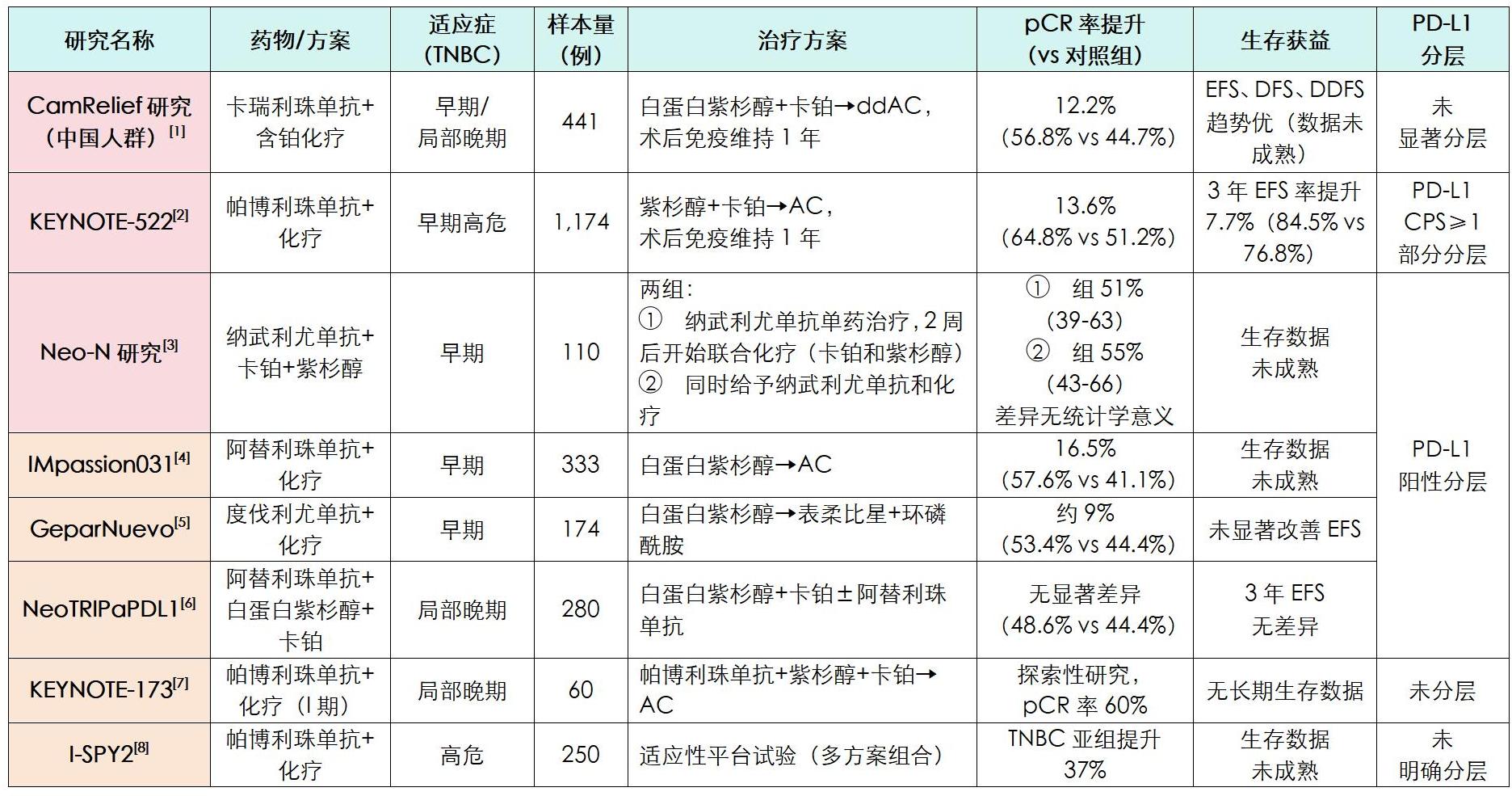
中國(guó)方案價(jià)值:CamRelief為T(mén)NBC新輔助治療提供了本土化證據(jù),而其他研究多以西方人群為主。
人群特異性:CamRelief是唯一100%納入中國(guó)TNBC患者的研究,且高危(III期/淋巴結(jié)陽(yáng)性)比例顯著高于其他研究。
治療方案:CamRelief采用劑量密集型AC(ddAC),可能增強(qiáng)療效;KEYNOTE-522和IMpassion031采用標(biāo)準(zhǔn)AC方案。
生存數(shù)據(jù):僅KEYNOTE-522和CamRelief顯示EFS獲益趨勢(shì),但CamRelief隨訪(fǎng)時(shí)間較短(14.4個(gè)月)。
PD-L1依賴(lài)性:CamRelief未顯示PD-L1表達(dá)與療效強(qiáng)相關(guān),而KEYNOTE-522和IMpassion031在PD-L1陽(yáng)性亞組獲益更顯著。
PD-L1表達(dá):PD-L1陽(yáng)性患者在免疫治療中收效更佳。KEYNOTE-522研究顯示,PD-L1 CPS≥1患者從帕博利珠單抗聯(lián)合化療中獲益更顯著。CamRelief研究觀察到PD-L1表達(dá)水平與pCR率之間的相關(guān)性,盡管未達(dá)到統(tǒng)計(jì)學(xué)顯著性,但在PD-L1 CPS≥10的患者中,卡瑞利珠單抗聯(lián)合化療組pCR率仍高于對(duì)照組。
不同化療方案與免疫治療的組合:不同研究采用不同的化療方案與免疫治療聯(lián)合。KEYNOTE-522研究中使用紫杉醇/卡鉑序貫多柔比星/環(huán)磷酰胺的方案,而CamRelief研究則采用白蛋白紫杉醇聯(lián)合卡鉑序貫表柔比星/環(huán)磷酰胺。研究均顯示免疫治療聯(lián)合化療在TNBC中的顯著療效,但具體的化療藥物選擇和劑量仍需根據(jù)患者的具體情況和研究證據(jù)進(jìn)行個(gè)體化調(diào)整。
免疫治療先給藥 vs 同步給藥:Neo-N研究創(chuàng)新性地設(shè)計(jì)免疫治療先給藥和同步給藥兩組方案。兩組的pCR率相近,但免疫治療先給藥組在PD-L1陽(yáng)性亞組中表現(xiàn)出更高的pCR率(70.6% vs 33.3%)。提示在特定生物標(biāo)志物指導(dǎo)下,免疫治療先給藥可能會(huì)帶來(lái)更好的療效,但需要更大樣本量的研究進(jìn)一步驗(yàn)證。
目前的研究為T(mén)NBC的免疫治療提供了豐富的證據(jù),但在實(shí)際臨床應(yīng)用中,仍需進(jìn)一步優(yōu)化治療方案。例如,如何根據(jù)患者的個(gè)體特征(如年齡、腫瘤分期、生物標(biāo)志物表達(dá)等)選擇最合適的免疫治療藥物和化療方案,以及確定******的治療周期和用藥順序,都是需要深入探討的問(wèn)題。
除了免疫治療與化療的聯(lián)合,未來(lái)還可探索免疫治療與其他治療手段的聯(lián)合應(yīng)用,如靶向治療、放療等,以進(jìn)一步提高TNBC患者的治療效果。例如,針對(duì)具有特定基因突變的TNBC患者,聯(lián)合HRD檢測(cè)及PARP抑制劑等靶向藥物可能帶來(lái)協(xié)同增效作用。
目前的臨床試驗(yàn)結(jié)果多基于理想的研究條件和入選標(biāo)準(zhǔn),而在真實(shí)世界中,患者的個(gè)體差異更大,合并癥更多,治療的依從性和耐受性也存在差異。因此,開(kāi)展真實(shí)世界研究,驗(yàn)證免疫治療在更廣泛人群中的療效和安全性,對(duì)于推動(dòng)其臨床應(yīng)用具有重要意義。
乳腺癌治療領(lǐng)域正經(jīng)歷著從傳統(tǒng)手段向精準(zhǔn)化、個(gè)體化治療的深刻變革。三陰性乳腺癌作為乳腺癌中最具挑戰(zhàn)性的亞型之一,免疫治療的興起為其帶來(lái)了新的曙光。通過(guò)不斷深入的研究和臨床實(shí)踐,我們有理由相信,未來(lái)將能夠?yàn)門(mén)NBC患者制定出更加優(yōu)化、高效的治療策略,進(jìn)一步提高其生存率和生活質(zhì)量,讓更多患者重獲健康與希望。
參考文獻(xiàn)
[1] JAMA. 2025 Feb 25;333(8):673-681.
[2] N Engl J Med. 2020 Feb 27;382(9):810-821.
[3] Lancet Oncol. 2025 Mar;26(3):367-377.
[4] Lancet. 2020 Oct 10;396(10257):1090-1100.
[5] Ann Oncol. 2022 Nov;33(11):1149-1158.
[6] ESMO Open. 2020 Mar;5(2):e000688.
[7] Ann Oncol. 2020 May;31(5):569-581.
[8] Curr Breast Cancer Rep. 2019 Dec;11(4):303-310.